Химический состав клеток
Белки
Белки - непериодические*, линейные гетерополимеры**, состоящие из аминокислотных остатков.
* - аминокислоты не чередуются регулярным образом.
** - состоят из разных аминокислот.
Длина белков
min 50 аминокислотных остатков (в инсулине)
max 26926 аминокислотных остатков (в титине - один из вспомогательных мышечных белков)
Мономеры
Мономеры молекулы низкомолекулярных соединений, способные в реакции полимеризации или поликонденсации превращаться в высокомолекулярные соединения.
Мономерами белков являются α (альфа) - аминокислоты.

R-радикал
1) Типы аминокислот:
ароматические
оксикислоты
серосодержащие и др.
2) Разновидности аминокислот:
Различают 20 разновидностей аминокислот, из них 8 незаменимые (лизин, лейцин, изолейцин, валин, триптофан, метионин, фенилаланин, треонин).
Примечание:
В действительности в состав природных аминокислот входят 22 аминокислот.
селеноцистеин (в животных тканях)
пирролизин (в архибактериях)
3) Химические свойства
Аминокислоты обладают кислотными и основными свойствами (амфотерны) и поэтому могут взаимодействовать друг с другом.
Реакция полимеризации
Химические и физико-химические свойстваполипептида.
дипептид
Молекула полипептида характеризуется полярностью: имеет два различных конца:
C-конец
N-конец
В клетке, на рибосоме наращивание полипептида происходит с N-конца.
Во многих радикалах ионогенные группы диссоцируя преобретают электрический заряд (гидрофильны). Молекула полипептида с многочисленными зарядами на поверхности покрывается гидратной оболочкой.
Именно этим объясняется хорошая растворимость некоторых белков в воде.
Пример: яичный альбумин.
Если в белке преобладают неполярные радикалы то он плохо растворим в воде.
Пример: эластин.
Первичная структура
Первичной структурой называетя последовательность* аминокислотных остатков в полипептидной молекуле.
* - для одних белков она видоспецифична.
Пример: инсулин у людей
для других индивидуально-специфична
Пример: белки тканевой совместимости.
Первичная структура закодирована в структурных генах (см. генетический код).
Конформация
1) Вторичная структура
Совокупность участков полипептидной молекулы, характеризующегося регулярной структурой.
Типы:
альфа - спираль
Правильная правозакрученная спираль возникающая в результате образования водородных связей между карбонильными и аминогруппами аминокислотных остатков (каждым первым и третьим).
Радикалы ориентированы от поверхности спирали.
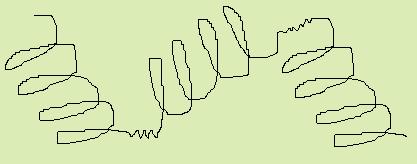
Пример: глобин - белковая часть гемоглобина.
бета - складчатая структура
Периодическая складчатая конфигурация, возникающая в результате образования водородных связей между параллельно-ориентированными участками одной или несколькихполипептидных молекул.
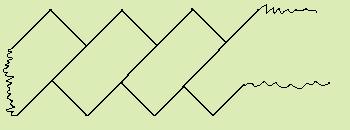
Пример: креотин волос и роговых элементов, фиброин щёлка.
Трёхчленная структура - особенная спиральчатая структура образовавшейся в результате сплетениятрёх полипептидных цепей.
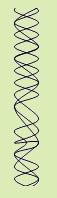
Пример: коллаген
Третичная структура
Пространственная организация белковой молекулы.
1) Типы:
глобулярная (шаровидая)
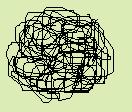
Пример: глобин
фибриллярная

Пример: миозин
Стабилизирующие силы
сильные связи: дисульфидная связь --S -S --
самые слабые: водородные, ионные, гидрофобные взаимодействия.
Неполярные R (радикалы) собираются в глубине белковой молекулы и формируют гидрофобные ядра.
Четвертичная структура
Образуется при объединении нескольких комплементарных молекул (субъединиц, протомеров) в комплекс. В комплекс могут входить одинаковые или различные протомеры. Поскольку такие комплексы характеризуются лабильностью (в процессе их функционирования имеют место переходы полимерных форм в протомерную и наоборот), стабилизирующие силы относяться слабым (водородные).
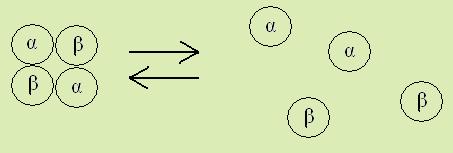
Пример: каталаза
Классификация
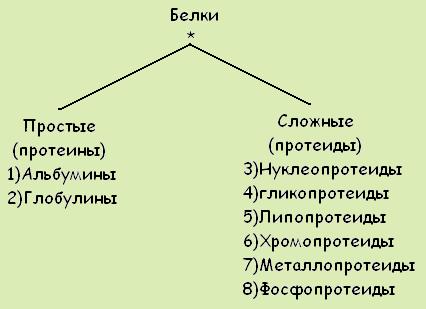
* - в зависимости от наличия или отсутствия в моекуле небелковой части.
Примеры:
1) Сывороточный альбумин (главный транспортный белок крови),
2) Гамма-глобулин (антитела)
3) ДНП (дизоксирибонуклеопротеид - основной компонент хрмосом), РНП (рибонуклеопротеид - основной компонент ядрышка)
4) Белки определяющие группу крови (гликофорины), находятся в мембранах эритроцитов,
5) ЛПНП, ЛПВП (липопртеиды низкой и высокой плотностей) играют важную роль в обмене холестерина. Он их соотношения зависит риск заболевания атероселерозом,
6) Гемоглобин
Неоглобин (окрашивает мышцы)
7) Трансферин - бело-переносчик железа, находится в плазме крови,
8) Казеин молока
Ихтулин рыбьей икры (содержит больше всего фосфопротеидов).
Функции белков 1)Каталитическая (ферментная) – каталитическая функция белков осуществляется с помощью специфических белков – катализаторов. Они ускоряют скорость биохимических реакций в десятки и сотни миллионов раз. 2)Сократительная (актин, миозин – основные мышечные белки). 3) Структурная (тубулины – белки микротрубочек, входящих в состав цитоскелета, керотины роговых структур). 4)Транспортная (транспортные белки биомембран; сывороточные альбумины). 5)Защитная (антитела) 6)Рецепторная (мембранные, цитоплазматические и ядерные рецепторы для гормонов; рецепторы для вирусов) 7) Регуляторная (пептидные гормоны: инсулин, гормон роста и др.). 8)Трофическая (белок эндосперма семян; фосфопротеиды рыбьей икры).
9)Энергетическая (при полном окислении 1 г. Белка освобождается 17,6 кДж энергии).
Химический состав клетки. Неорганические вещества
Атомный и молекулярный состав клетки. В микроскопической клетке содержится несколько тысяч веществ, которые участвуют в разнообразных химических реакциях. Химические процессы, протекающие в клетке,одно из основных условий ее жизни, развития и функционирования.
Все клетки животных и растительных организмов, а также микроорганизмов сходны по химическому составу, что свидетельствует о единстве органического мира.
Содержание химических элементов в клетке
Элементы Количество (в %) Элементы Количество (в %)
Кислород 65-75 Кальций 0,04-2,00
Углерод 15-16 Магний 0,02-0,03
Водород 8-10 Натрий 0,02-0,03
Азот 1,5-3,0 Железо 0,01-0,015
Фосфор 0,2-1,0 Цинк 0,0003
Калий 0,15-0,4 Медь 0,0002
Сера 0,15-0,2 Йод 0,0001
Хлор 0,05-0,1 Фтор 0,0001
Выше приведены данные об атомном составе клеток. Из 109 элементов периодической системы Менделеева в клетках обнаружено значительное их большинство. Особенно велико содержание в клетке четырех элементов - кислорода, углерода, азота и водорода. В сумме они составляют почти 98% всего содержимого клетки. Следующую группу составляют восемь элементов, содержание которых в клетке исчисляется десятыми и сотыми долями процента. Это сера, фосфор, хлор, калий, магний, натрий, кальций, железо. В сумме они составляют 1.9%. Все остальные элементы содержатся в клетке в исключительно малых количествах (меньше 0,01%)
Таким образом, в клетке нет каких-нибудь особенных элементов, характерных только для живой природы. Это указывает на связь и единство живой и неживой природы. На атомном уровне различий между химическим составом органического и не органического мира нет. Различия обнаруживаются на более высоком уровне организации - молекулярном.
